PAHO / WHO
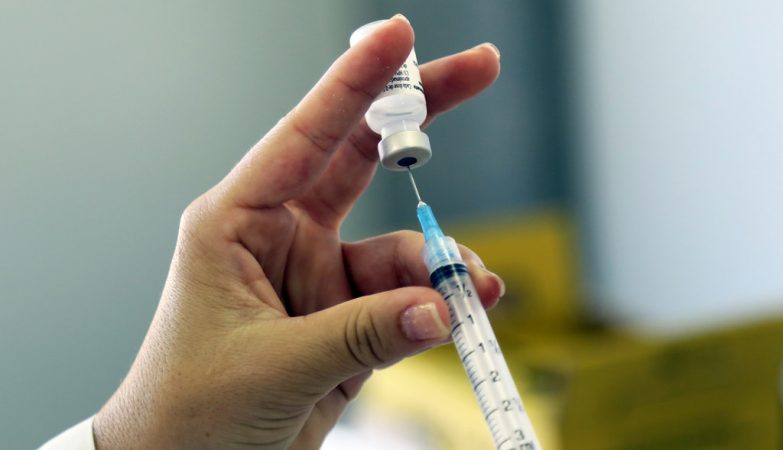
A Agência Europeia de Medicamentos (EMA) aprovou “sob condições” nesta segunda-feira a vacina contra a Covid-19 da Pfizer-BioNTech. Os países da União Europeia pretendem começar a imunização no dia 27 de dezembro.
“Eu estou feliz em anunciar que o comitê científico da EMA se reuniu hoje e foi favorável à autorização para a venda condicional na União Europeia da vacina desenvolvida pela Pfizer e BioNTech”, afirmou Emer Cooke, diretora geral da agência reguladora.
O anúncio da aprovação foi feito após uma reunião antecipada do Comitê de Medicamentos de Usos Humanos. O encontro estava previsto para 29 de dezembro, mas mudou de data após a pressão da Alemanha e de outros países europeus, que veem um aumento de casos de Covid-19 devido à chegada do inverno no Hemisfério Norte.
A Comissão Europeia deve agora aprovar esta decisão para dar início à campanha de vacinação em todo o bloco econômico, que conta quase 450 milhões de habitantes. A expectativa é de que as primeiras doses sejam aplicadas já no próximo domingo (27).
A vacina desenvolvida pela gigante americana Pfizer e a empresa alemã BioNTech demonstrou eficácia de 95% nos testes clínicos internacionais em que foram administradas duas doses com três semanas de intervalo.
O imunizante já está sendo administrado em outros países, como os Estados Unidos, Reino Unido e Israel, e centenas de milhares de pessoas já tomaram a vacina, com raros casos de reação alérgica.
Aprovação diante de nova linhagem do vírus
A aprovação é anunciada um dia após diversas nações europeias decidirem fechar suas fronteiras com o Reino Unido por conta da descoberta de uma nova linhagem de coronavírus que está circulando no país.
A variante do vírus poderia ser até 70% mais contagiosa, segundo afirmou o premiê britânico no último sábado.
A princípio, a vacina da Pfizer/BioNTech também funcionaria contra a Covid-19 desenvolvida a partir dessa nova mutação.
“Até o momento, não há qualquer prova sugerindo que a vacina não seja eficaz contra a nova linhagem”, garantiu a diretora da agência europeia Emer Cooke.
Demora para aprovação
Vários países reclamaram da lentidão do processo de decisão da agência europeia, incluindo Alemanha, Polônia e Hungria.
A agência europeia afirma ter feito uma “análise contínua” dos dados procedentes das análises dos laboratórios e testes clínicos à medida que eram enviados. Em um período normal, a agência só examina os dados após o envio de todas as informações.
A Pfizer/BioNTech apresentou no dia 1° de dezembro uma solicitação de autorização. Desde então, Reino Unido, Estados Unidos e Canadá aprovaram o uso emergencial e iniciaram campanhas de vacinação.
Após antecipar a decisão para a primeira vacina contra a Covid-19, a agência também deverá tomar uma decisão antecipada em relação à vacina do laboratório Moderna, já aprovada nos Estados Unidos. O Comitê europeu deve se pronunciar sobre o imunizante na primeira semana de janeiro.
// RFI