Osnei Restio / Prefeitura de Nova Odessa
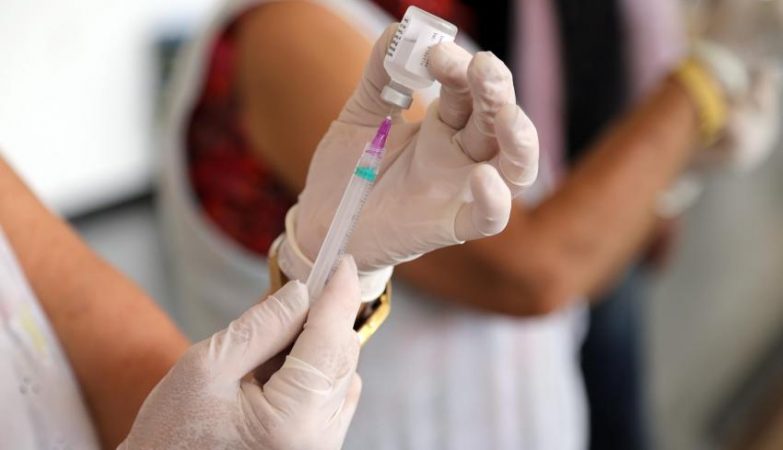
Dividiu opiniões a decisão do Ministério da Saúde de suspender a vacinação de grávidas contra a Covid 19, qualquer que seja o imunizante, numa medida que foi além da orientação da própria Agência Nacional de Vigilância Sanitária (Anvisa).
Por enquanto, apenas gestantes com comorbidades deverão receber as doses, desde que não sejam as da Oxford/AstraZeneca, devido a um possível e raro caso de trombose aguda que pode ter matado uma grávida no Rio de Janeiro.
Como as gestantes têm se mostrado um grupo de risco, entraram mês passado na lista de prioridades. Especialistas consideraram excessiva a postura do ministério.
“A decisão de interromper a vacinação de grávidas sem comorbidade no Brasil, com todas as vacinas disponíveis, me parece uma medida muito restritiva e exagerada para o momento e para o evento que ocorreu. Entendo que a investigação do caso deva se fazer cautelosamente, interrompendo a vacinação com a vacina da AstraZeneca. Mas não vejo motivo para a interrupção com os outros imunógenos”, disse à RFI o médico Érico Arruda, consultor da Sociedade Brasileira de Infectologia.
Já Dalcy Albuquerque, da Sociedade Brasileira de Medicina Tropical, afirmou à RFI que o governo optou pela prudência e não dá para dizer que errou na dose.
“Acho que neste momento é difícil entrar no mérito dessa questão, porque estamos bem no meio do que aconteceu. Ainda não está bem apurada a morte dessa paciente, se teria sido efeito colateral da vacina. O próprio ministério, ao suspender, se comprometeu de nos próximos dias soltar diretrizes novas. Acho que neste momento é uma decisão que a gente tem que observar. Acho que não dá para dizer se está certa ou errada. Foi uma decisão prudente, inclusive com outras implicações até para não correr o risco de você assustar as pessoas, ou as pessoas fugirem da vacinação.”
Imagem
Uma das análises é a de que o governo tenta também preservar a imagem da vacina da AstraZeneca porque ela é hoje o principal imunizante aplicado no Brasil.
Numa coletiva à imprensa na noite dessa terça-feira (11), o Ministério da Saúde convidou médicos que integram um grupo de assessoramento da campanha de vacinação para destacar a confiança das vacina aplicadas no país.
“A população precisa se vacinar. E essa vacina da Oxford/AstraZeneca é muito boa, usada em vários países e hoje é o que temos em maior quantidade para avançarmos nessa imunização”, afirmou o médico e pesquisador Jorge Kalil.
Das gestantes já vacinadas, 15 mil receberam a vacina da AstraZeneca, 3.900 a da Pfizer e 3.400 a Coronavac. Outros eventos adversos possivelmente relacionados a essas vacinas estão sendo apurados, mas segundo o governo não descreditam a qualidade dos produtos.
Butanvac
O Butantan deve enviar ao Ministério da Saúde esta semana quatro milhões de doses da Coronavac, do laboratório chinês Sinovac, totalizando 46 milhões até aqui. Só que dez mil litros de insumos aguardam liberação na China para garantir a produção de novas doses, e o país exportador, ainda assim, tem sido alvo de críticas constantes do clã Bolsonaro.
Para reduzir essa dependência, o governo espera contar, a partir de agosto, com a produção do IFA no Brasil e também dispor de um imunizante nacional até o ano que vem. Muitos apostam que a vacinação contra o coronavírus necessitará de doses de reforço.
São vários projetos em andamento, como a Butanvac, que está sendo desenvolvida pelo Butantã em São Paulo e depende agora de uma autorização da Anvisa para começar a próxima fase: o teste em humanos. O governo paulista fala em ter a vacina para distribuição até setembro.
“Observamos, na análise inicial, alguns pontos que precisavam de melhor esclarecimento. Já oficiamos ao desenvolvedor e estamos agora aguardando o retorno deles para que o processo continue. Temos a Butanvac e temos também a Versamune, que são vacinas que estão, neste momento, em análise de estudo clínico fase 2 e 3 com a Anvisa”, observou o presidente da Anvisa Antonio Barra Torres, ao responder a questionamentos na CPI da Covid no Senado.
Investimento em ciência
Para a comunidade científica, a pandemia confirmou que investir em pesquisa faz muita diferença e o Brasil, que é um player importante na produção de vacinas, acumulou gargalos e acabou perdendo espaço para laboratórios da China e da Índia.
O pesquisador do Instituto de Ciências Biológicas da UFMG, Sérgio Costa, trabalha em duas vacinas contra a Covid. Uma delas usa uma proteína recombinante e já passou pela primeira etapa dos testes em animais. A outra utiliza como vetor a bactéria da tuberculose, técnica parecida com a da AstraZeneca, mas que no lugar de um adenovírus usa-se a BCG, bactéria já bem conhecida, que não oferece riscos e é cultivada nos laboratórios de universidades.
Além disso, o estudo pode ser bem promissor pelas capacidades desse microrganismo de estimular o sistema imunológico de forma geral. “Esse trabalho traz vantagens e se apresenta como potencial importante na área de vacinas. E esse imunizante seria bivalente, combatendo o coronavírus e também a tuberculose”.
Sérgio Costa lamenta, no entanto, que o país só tenha dado importância ao trabalho científico agora, no meio da pandemia mais agressiva já vivida pelo país. “E o grande problema é a falta de continuidade de investimento em pesquisa básica e pesquisa aplicada, desenvolvimento científico e tecnológico no Brasil nos últimos anos.
Na realidade o Brasil necessita de um investimento contínuo para que esses grupos de pesquisa continuem investigando, desenvolvendo seus produtos e suas tecnologias para que, quando haja uma pandemia ou outro evento que na realidade coloque em risco a nossa sociedade, a gente tenha rapidez em buscar soluções que são necessárias para o controle de uma enfermidade como a Covid-19.”
O professor da UFMG considera difícil o país contar com um imunizante totalmente nacional já a partir deste ano.
“Eu não acredito que o Brasil terá uma vacina nacional ainda este ano. Existem três projetos mais avançados, que devem ter continuidade, mas este ano não acredito. Na realidade, se vocês forem observar, alguns desses projetos produzem algum material, alguma forma da vacina recombinante fora do Brasil, o que já é por si uma limitação. Eu acho que a gente precisa desenvolver, ter plataformas de tecnologia no Brasil para produção por exemplo de moléculas recombinantes em sistema de boas práticas de fabricação, que é requerido para se chegar até o ensaio clínico de fase 1 e 2. Hoje a gente tem na realidade dificuldade de importação de insumos, importação de reagentes para o desenvolvimento de projetos de pesquisa e também para a produção de vacinas.”
// RFI